近日,国际顶级期刊Accounts of Chemical Research报道了北京理工大学黄渊余教授课题组在克服核酸药物发展瓶颈方面发表的综述文章,该论文以“Overcoming pharmaceutical bottlenecks for nucleic acid drug development”为题,被选为期刊的Supplementary Cover进行发表。文章的第一作者为北京理工大学前沿交叉科学研究院陆梅研究员和国家纳米科学中心邢昊楠博士,通讯作者为北理工黄渊余教授和国家纳米科学中心梁兴杰研究员(北理工兼职教授),北理工为论文第一单位。

新型冠状病毒的大流行及两种mRNA疫苗的迅速获批使得核酸药物引起了社会的广泛关注。过去几年里,多种核酸疗法的批准呈加速趋势,标志着核酸领域的发展已进入一个崭新的时代。然而,核酸药物一些不利的理化及生物特性,如荷负电、分子量大、亲水、对核酸酶降解敏感、存在脱靶副作用及免疫原性等,仍是制约核酸药物开发与产业化的阻力。因此,核酸制药领域亟待开发新技术以提高核酸药物的稳定性、靶向性、入胞效率、内溶酶体逃逸,进而提高其疗效和安全性。
北理工黄渊余教授、陆梅研究员与国家纳米科学中心梁兴杰研究员、邢昊楠博士等从核酸药物在体内的稳定性、靶向与入胞、内涵体逃逸及核酸序列设计与修饰等方面,概述了核酸药物开发的前沿技术平台(图1)。
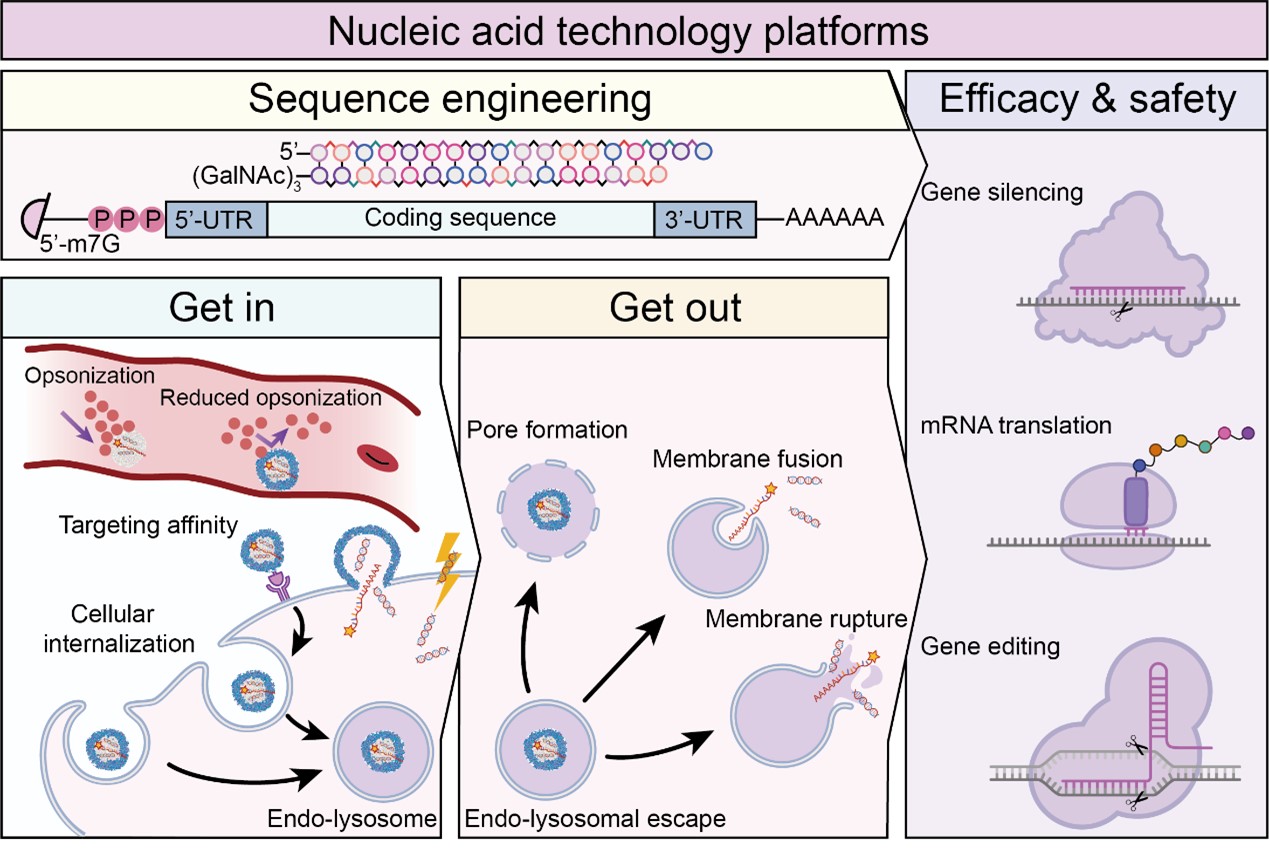
图1 核酸药物技术平台:序列设计、修饰与递送技术
一、克服“进得去”瓶颈的策略
通过设计多种智能核酸递送平台,如聚合物、脂质纳米颗粒(LNP)和无机纳米颗粒等合成纳米材料,电穿孔等物理递送方法及外泌体等天然递送载体,提高核酸药物的循环稳定性及靶组织的入胞效率(“进得去”)。例如,团队设计了常规碳链和氟化碳链组成的低聚乙烯亚胺(OEI)纳米组装体,研究其在无血清和有血清环境下的siRNA递送效率和机制,证明氟化OEI可显著降低非特异性血浆蛋白吸附,提高在有血清环境下的入胞效率和基因沉默效率(图2)。
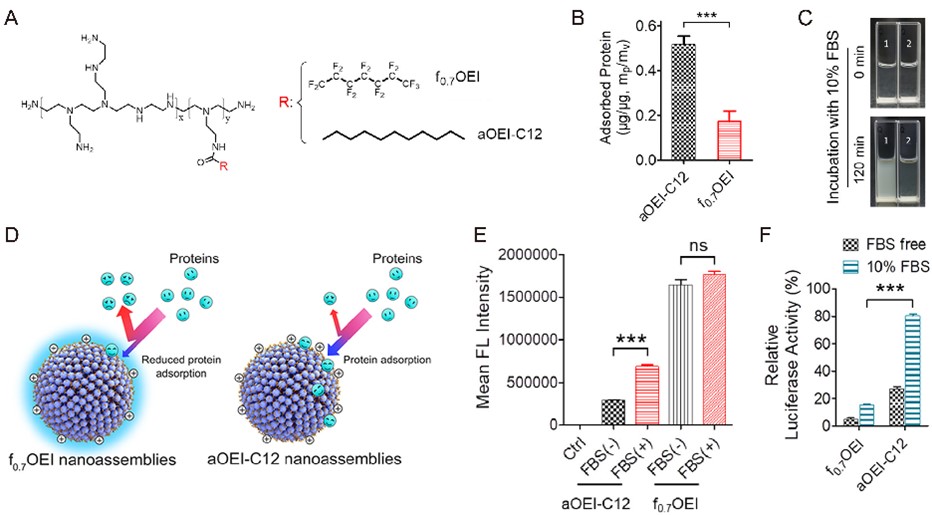
图2. 氟化对siRNA入胞与基因沉默效率的影响
通过电穿孔、膜融合等策略可使核酸直接抵达细胞质,提高递送效率。例如,通过设计系列电穿孔芯片和器件,在低电压下实现细胞和活体组织膜穿孔,使siRNA直达胞质(图3)。
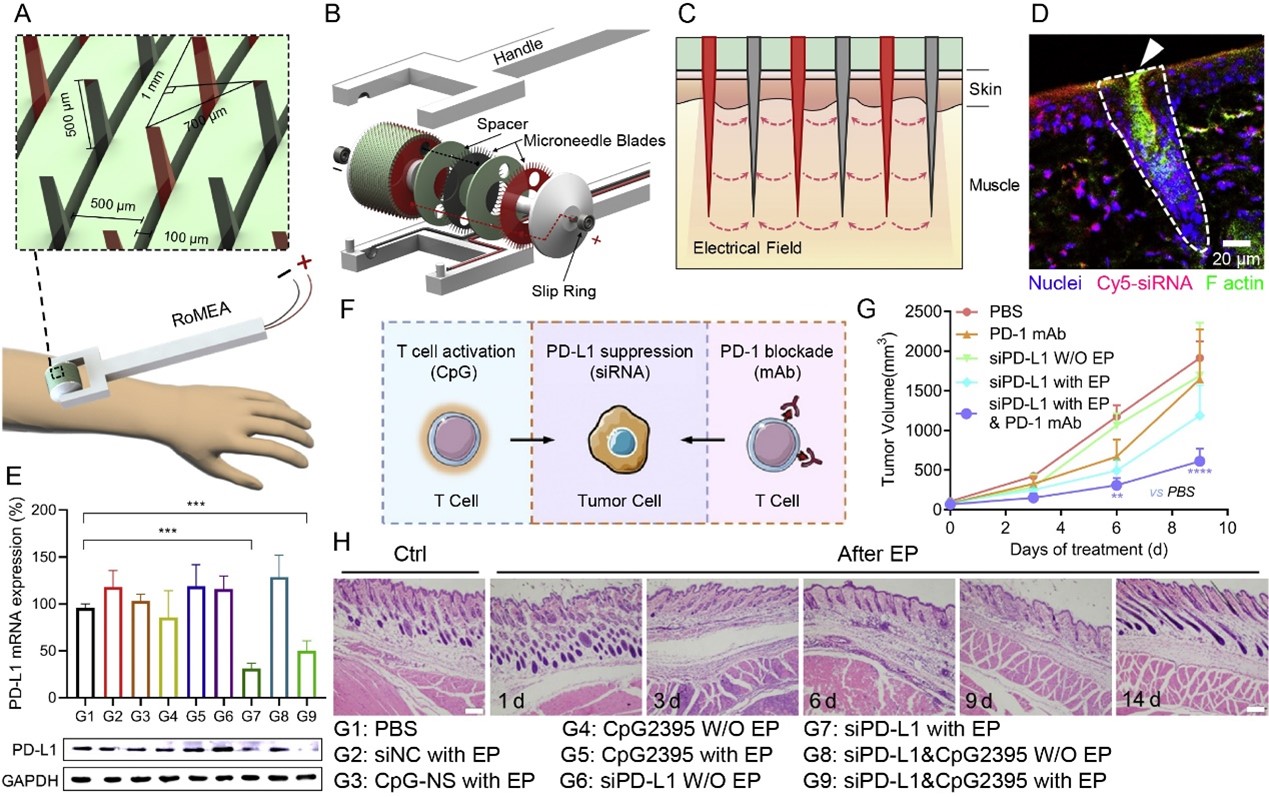
图3. 新型电穿孔芯片或器件在低电压脉冲下,介导核酸通过膜穿孔入胞
利用疱疹性口腔炎病毒糖蛋白G(VSV-G)改造M1型巨噬细胞来源的外泌体,实现在微酸的肿瘤微环境下,VSV-G介导与靶细胞膜融合入胞,实现高效基因抑制和肿瘤免疫治疗(图4)。
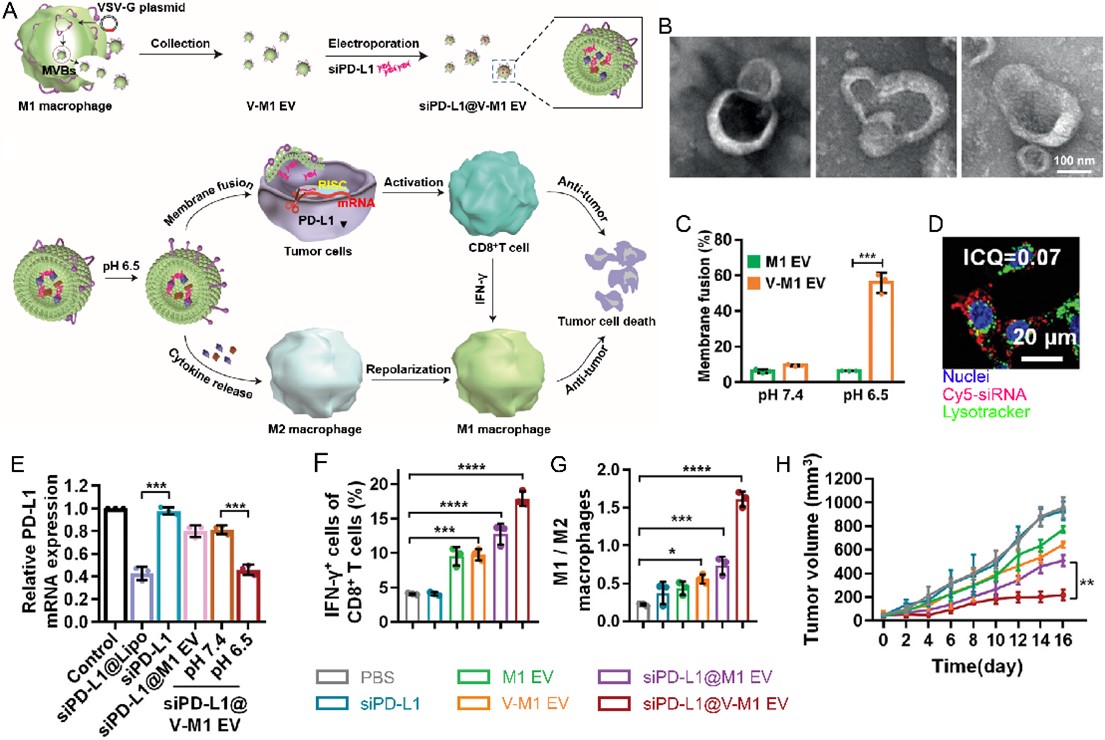
图4. VSV-G修饰的M1巨噬细胞外泌体递送siRNA抗肿瘤
通过三螺旋寡核苷酸(TFO)诱导尺寸小于10 nm金颗粒的自组装,设计了DNA纳米花,最终协同超细金纳米颗粒的入核能力和较大纳米颗粒的肿瘤蓄积特性,在近红外光照射下释放出反义寡核苷酸、实现细胞核内高效的基因抑制(图5)。
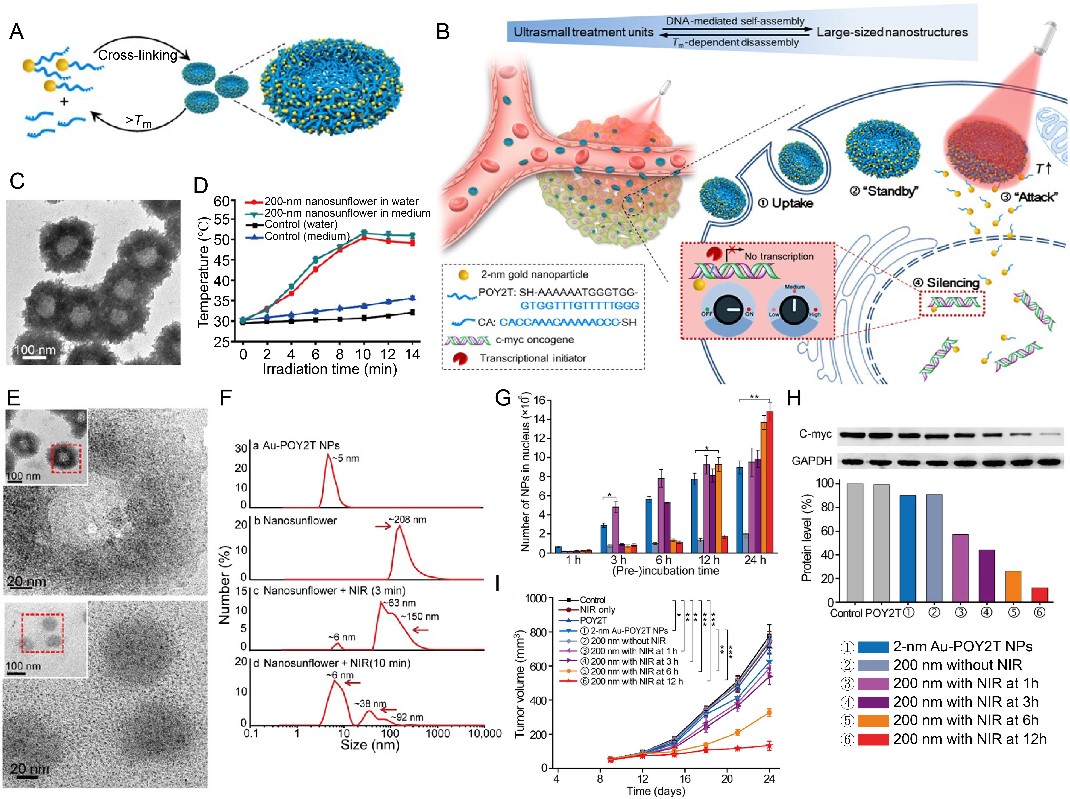
图5. 自组装金-DNA纳米花介导核内基因抑制
二、克服“出得来”瓶颈的策略
其次,作者概述了多种内涵体逃逸策略,如pH敏感纳米材料(聚合物、多肽、电荷翻转材料等)、水解酶敏感纳米载体、光化学内化策略(活性氧破膜)、内涵体溶解剂(如氯喹)及膜融合蛋白/多肽等,以提高核酸药物的内溶酶体逃逸效率(“出得来”)。例如,设计pH敏感、聚阳离子三嵌段共聚物胶束(GDDC-Ms),实现在酸性内涵体/溶酶体环境中通过质子海绵效应高效破膜、逃逸内涵体。发现尽管GDDC-Ms的胞吞效率较低,其在50 nM的siRNA浓度下的基因抑制率可达98.8%,优于市售转染试剂Lipofectamine 2000(图6)。
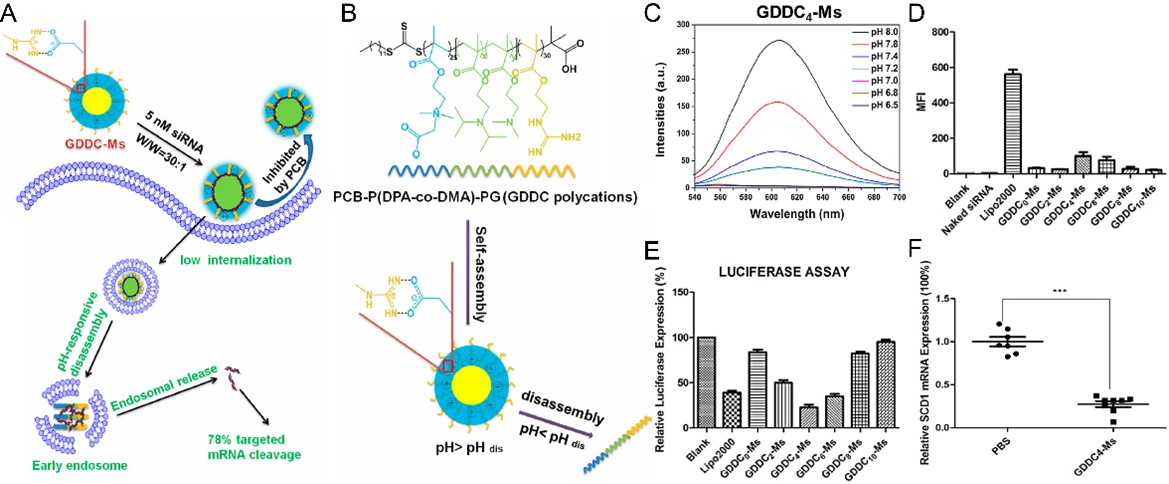
图6. pH敏感聚合物纳米胶束的内涵体逃逸与基因抑制率
可离子化脂质的的头部基团(如氨基、胍基及杂环基团等)在酸性条件下可发生质子化带正电,借助该特性可离子化脂质可与内涵体/溶酶体膜上荷负电的脂质发生相互作用,进一步引起膜失稳、破裂。团队利用该机制设计了一系列新型LNP应用于核酸递送,促进内涵体逃逸(图7)。
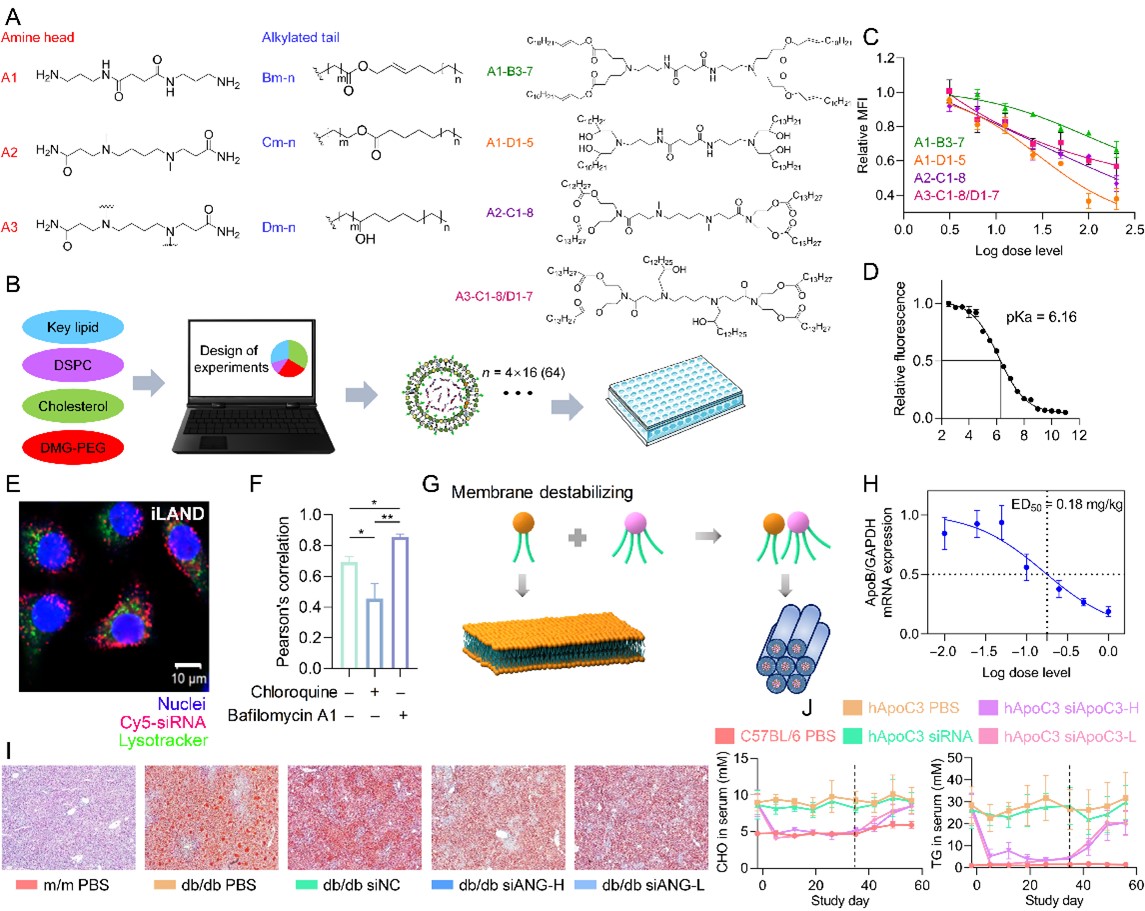
图7. 可离子化脂质纳米颗粒递送siRNA治疗高血脂
三、核酸序列设计与修饰
最后,作者介绍了核酸序列设计与化学修饰策略方面的研究进展,旨在增强核酸药物的核酸酶抗性、翻译效率,并减轻其脱靶毒性和免疫原性。例如,团队系统研究与阐述了siRNA降解机制,发现核酸酶对siRNA的降解主要发生在UA/UA和CA/UG配对位点,增强修饰的裸siRNA具有良好的血清稳定性,单次给药药效持续数月。同时,提出了系列mRNA的增稳定、促翻译及降免疫原性策略,提高了mRNA的翻译水平。
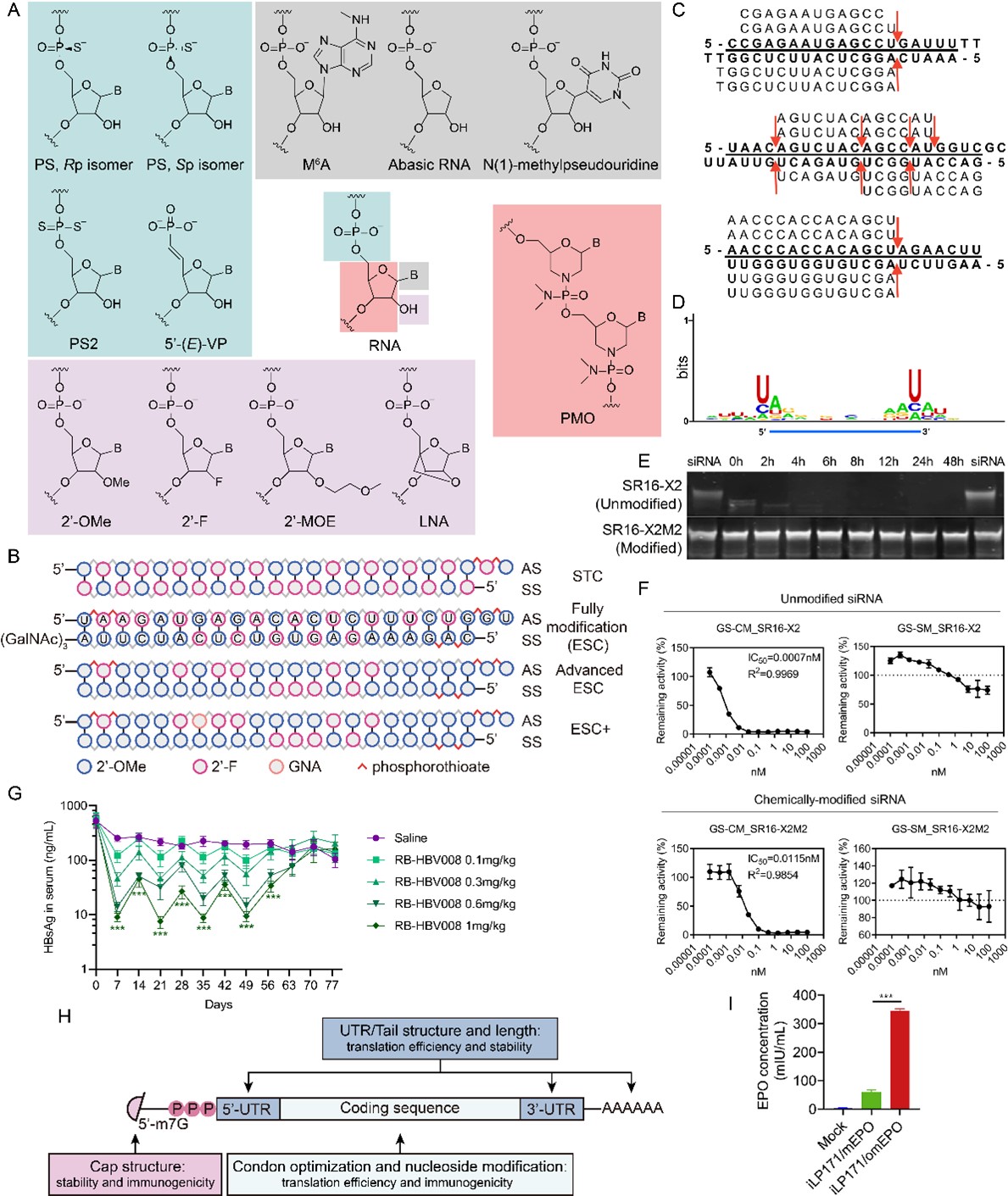
图8. 核酸序列设计与修饰策略
参考文献:
Mei Lu#, Haonan Xing#, Aiping Zheng, Yuanyu Huang*, Xing-Jie Liang*. Overcoming pharmaceutical bottlenecks for nucleic acid drug development. Acc. Chem. Res., 2023, 56, 224-236.
论文链接: https://pubs.acs.org/doi/10.1021/acs.accounts.2c00464
作者简介:
梁兴杰,国家纳米科学中心研究员,北京理工大学兼职教授,博导,中国科学院“百人计划”研究员,国家级领军人才、美国医学与生物工程院(AIMBE)Fellow、973重大研究计划项目首席科学家。主要从事纳米结构的生物学效应,以及设计构建纳米药物提高药物输送效率并研究其克服临床适应性耐受的作用机制。已在Nat Nanotech, PNAS,Sci Adv、Nat Commun、Adv Mater等学术期刊发表论文300余篇,文章引用率超25000次,H-index > 86。现担任《Exploration》主编,《Biomaterials》期刊副主编等学术职务。
黄渊余,北京理工大学教授,博导,国家级青年人才、斯坦福大学全球前2%顶尖科学家(连续三年)、北京市科技新星,获得北京市自然科学一等奖(第九)、广西自然科学一等奖(第五)、中美纳米医学与纳米生物技术学会“未来之星”等荣誉。主要围绕核酸技术与药物/疫苗开展研究,以第一/通讯作者在Sci Adv、Signal Transduct Target Ther、Adv Mater、Adv Sci、Nano Today等期刊发表论文近70篇,共发表论文100余篇;申请专利20余件;作为课题或项目负责人承担国家重点研发计划、国家自然科学基金等项目10余项。中国生物物理学会纳米生物学分会秘书长, Exploration创刊副主编(Wiley出版)、多个期刊(青年)编委。
陆梅,北京理工大学研究员,博导,主要从事外泌体核酸(siRNA、mRNA等)药物与疫苗相关研究。目前,以第一/通讯作者在Acc Chem Res、Adv Mater、Biomaterials、Acta Pharm Sin B、Acta Biomater等学术期刊发表论文20余篇,ESI高被引论文1篇,封面论文1篇,顶级SCI期刊论文11篇,申请专利2件。作为课题或项目负责人承担国家自然科学基金、北京市自然科学基金等项目4项,作为学术骨干参与国家重点研发计划及国家自然科学基金等项目2项。获得沈阳市自然科学学术成果奖二等奖(第二)等荣誉。Exploration期刊青年编委,美国细胞外囊泡协会(AAEV)Fellow,中国生物材料学会及中国抗癌协会纳米肿瘤分会会员,Biomaterials、Int J Pharm、Curr Pharm Design等期刊审稿人。
课题组主页: https://www.x-mol.com/groups/Yuanyu_Huang-BIT